Chez Tedisel Medical, nous sommes fiers de proposer l’une des meilleures offres d’équipements hospitaliers sur le marché. Nos dispositifs médicaux sont entièrement conformes aux normes européennes et internationales en matière de gestion de la qualité, de fabrication et de conception, ainsi qu’au marquage CE.
Ce marquage CE est la porte d’entrée pour la commercialisation de produits médicaux dans l’Union européenne.
Examinons maintenant en détail en quoi il consiste et quelles sont ses caractéristiques, ainsi que les principales réglementations applicables aux dispositifs médicaux.
Qu’est-ce que le marquage CE?
Le marquage CE de conformité sanitaire, comme nous l’avons dit, est une exigence obligatoire pour la commercialisation des dispositifs médicaux en Europe. Il est indiqué sur leur étiquetage et leurs instructions d’utilisation par le symbole CE + numéro d’organisme notifié.
Ce marquage CE de santé indique la conformité du produit avec les directives qui lui sont applicables. Ainsi, il est illégal en Europe de commercialiser et d’utiliser ultérieurement des produits qui ne portent pas ce marquage.
Au moyen du marquage CE, le fabricant de dispositifs médicaux indique également et atteste que son produit est conforme aux exigences générales de sécurité et de performance (GSPR) de toutes les réglementations européennes applicables aux dispositifs médicaux.
Il s’agit de l’une des certifications les plus complexes car elle doit être conforme à toutes les directives européennes pertinentes.

Certificat CE pour les dispositifs médicaux – une garantie
Les directives établissent des exigences minimales pour l’évaluation et la certification des produits ainsi que pour le marquage CE. À cet égard, la directive oblige tous les fabricants à fournir les garanties suivantes:
- Garantie d’information: Une documentation technique du produit doit être établie.
- Garantie de sécurité: Tester l’équipement conformément aux réglementations applicables et à sa classification.
- Garantie de conformité aux spécifications et à l’efficacité: Évaluation clinique et, le cas échéant, recherche clinique pour évaluer la sécurité et la conformité aux spécifications du produit.
- Assurance qualité: L’entreprise doit mettre en place un système d’assurance qualité conforme à la norme ISO 13485 (nous en discuterons plus en détail ultérieurement) avec un suivi correspondant pour garantir sa mise en œuvre correcte
Étapes pour obtenir la certification CE
ÉTAPE 1
Pour obtenir le certificat européen de conformité, nous devons d’abord classer le dispositif médical afin de respecter les exigences spécifiques qui lui sont applicables, notamment le type de produit et les risques.
ÉTAPE 2
Ensuite, nous préparerons le dossier technique (Dossier Technique) : gestion des risques, essais cliniques, validation des processus, etc.
ÉTAPE 3
Enfin, il est temps de présenter le dispositif médical à un organisme notifié, qui effectuera un audit et décidera de son marquage CE et de sa commercialisation dans les pays de l’Union européenne.
Quelles sont les réglementations européennes pour les dispositifs médicaux?
Le Règlement de l’UE 2017/745 relatif aux dispositifs médicaux (règlement sur les dispositifs médicaux ou MDR) est, depuis son entrée en vigueur en mai 2021, la réglementation européenne qui stipule qu’aucun dispositif médical ne peut être commercialisé sur le territoire européen sans le marquage CE.
Cette loi couvre tous les acteurs de la scène médicale : fabricant, distributeur, médecin, opérateur et patient, car un seul d’entre eux ne peut garantir la sécurité et l’efficacité des produits.
Ainsi, certaines des nouvelles fonctionnalités introduites par cette récente réglementation européenne sont:
- Création d’une nouvelle base de données appelée EUDAMED garantissant la transparence et permettant aux autorités, à l’industrie, aux professionnels de la santé et au grand public d’accéder aux informations sur les dispositifs médicaux disponibles sur le marché européen.
- Amélioration de la traçabilité des dispositifs médicaux, grâce à la mise en place d’un numéro d’identification unique (UDI).
- Renforcement du processus de désignation et de supervision des organismes notifiés.
- Exigences plus strictes concernant les données précliniques et cliniques que les dispositifs médicaux doivent avoir avant d’obtenir le marquage CE.

Réglementation et surveillance du marquage CE en Espagne
En Espagne, l’Agence espagnole des médicaments et des produits de santé (AEMPS, rattachée au ministère de la Santé et de la Politique sociale) est l’organisme qui certifie que ces articles à usage clinique sont conformes à la Directive sur les dispositifs médicaux.
Les principales réglementations pour les dispositifs médicaux
Dans n’importe quelle industrie, les normes sont le moyen le plus sûr de garantir la conformité des produits et d’harmoniser les exigences tant au niveau national qu’international. Le secteur de la santé est peut-être l’industrie où la conformité des produits est la plus cruciale, tant dans la conception que dans la fabrication des dispositifs médicaux.
L’industrie des dispositifs médicaux est responsable de la conception et de la fabrication d’une large gamme de produits utilisés pour diagnostiquer et traiter les maladies et améliorer la santé des patients.
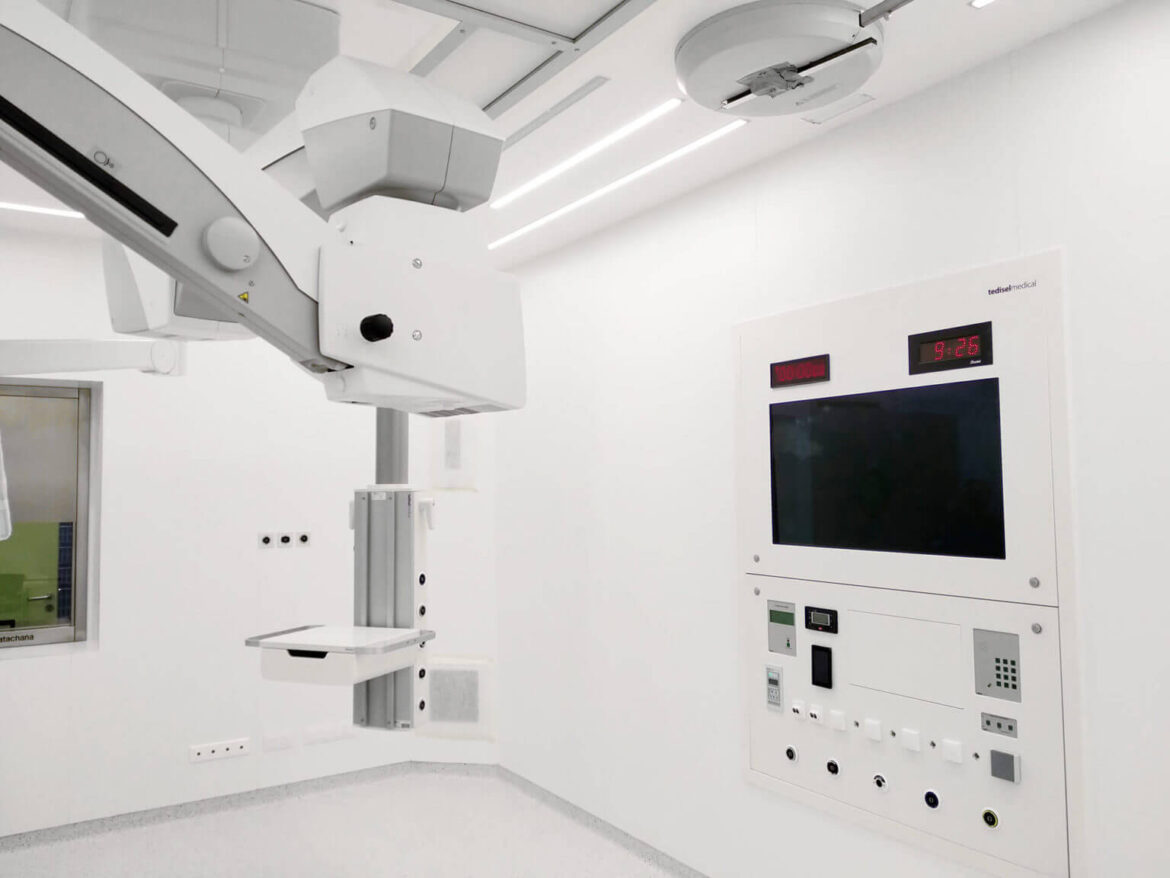
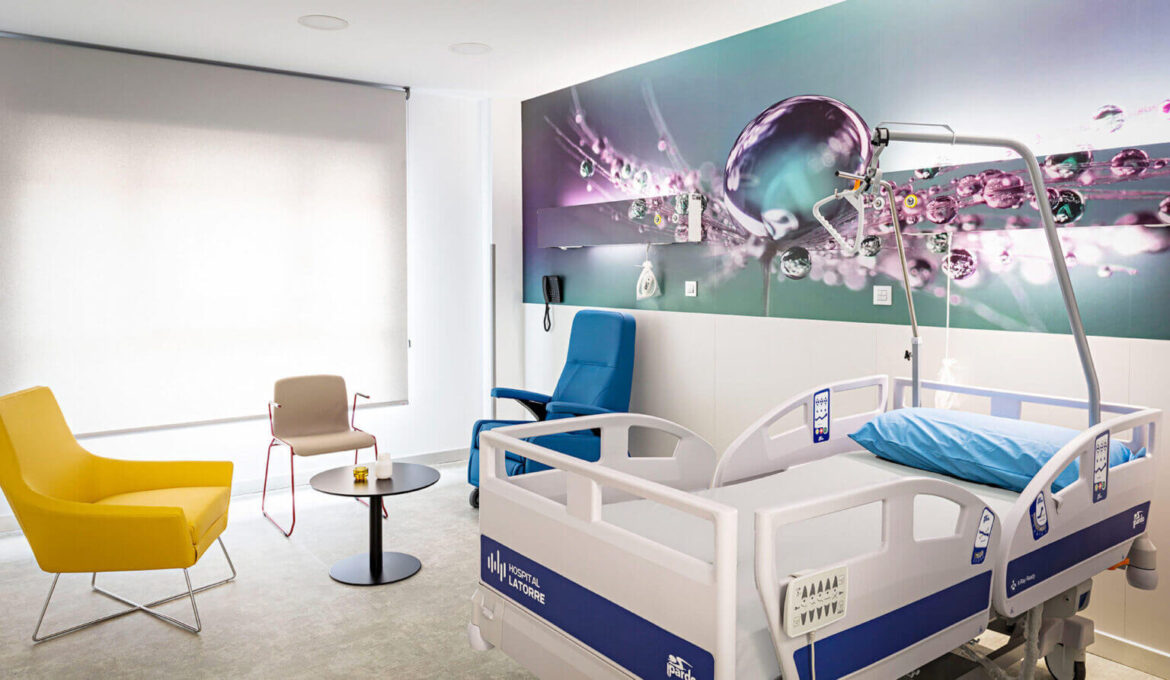
Les produits vont des équipements d’imagerie, des têtes de lit, des suspensions, des panneaux techniques ou des logiciels aux prothèses articulaires et autres implants.
Ainsi, comme les dispositifs médicaux sont des outils essentiels pour les soins de santé et que ces produits ont un impact direct sur la santé publique et la qualité de vie, leur sécurité est impérative. Pour obtenir les résultats requis et éviter les rappels de dispositifs, les entreprises doivent suivre les normes de fabrication des dispositifs médicaux.
Le système ISO
Bien qu’il existe plusieurs normes de gestion applicables à la fabrication de dispositifs médicaux, la norme ISO est la plus pertinente à l’échelle mondiale pour l’environnement médical. Grâce à elles, nous pouvons connaître la qualité, la conception, la capacité de travail ou le développement technique et technologique d’un fabricant. Les plus courantes sont les suivantes:
- ISO 13485 : Il s’agit du système de gestion de la qualité spécialement conçu pour les fabricants de produits médicaux. Il constitue une extension et un affinement du cadre établi par l’ISO 9001, qui est la norme générale de gestion de la qualité pour toutes les industries et secteurs. La conformité à l’ISO 13485 contribue au contrôle global de la qualité, à la traçabilité, à la validation des processus et à la gestion des risques. Elle est destinée et conçue pour être utilisée dans les organisations impliquées dans la conception et le développement, la production, l’installation, le service et la vente de dispositifs médicaux.
Une organisation certifiée démontre sa capacité à fournir des dispositifs médicaux et des services associés qui répondent constamment aux exigences des clients et aux réglementations applicables. Les fabricants qui obtiennent la conformité à l’ISO 13485 trouveront plus facile d’introduire leurs produits sur les marchés internationaux. La conformité peut également rationaliser vos processus et vous aider à gérer une opération plus efficace, rentable et moins risquée.
- ISO 14001: Cette norme est axée sur la durabilité et la mise en place d’un système de gestion environnementale qui peut aider les fabricants de dispositifs médicaux à réduire les déchets, à conserver l’énergie et à réduire leur empreinte carbone globale.
- ISO 45001: Il s’agit de la norme sur les risques professionnels spécifiques et la sécurité au travail dans l’industrie des dispositifs médicaux.
- ISO 27001: Il s’agit de la norme pour la sécurité des données, c’est-à-dire la cybersécurité.

Normes IEC 60601
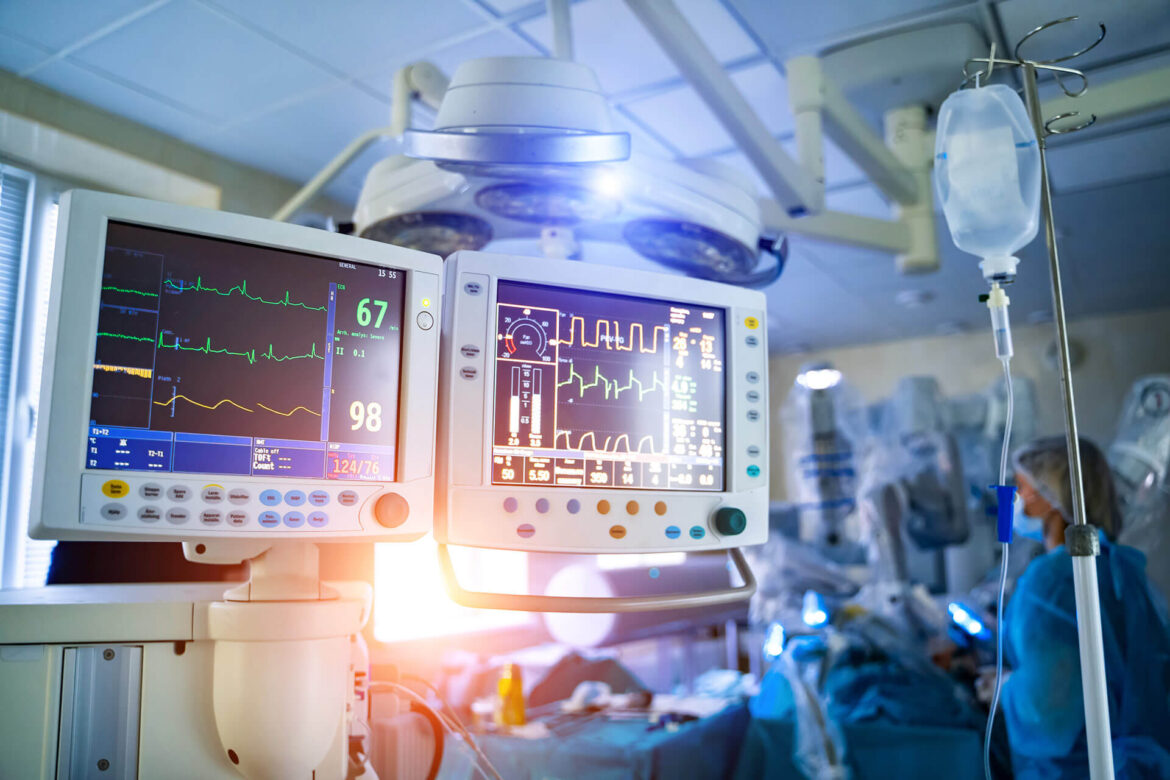
Les normes IEC 60601 sont déjà largement acceptées par les autorités sanitaires de différents pays tels que les États-Unis, la Russie, le Japon, le Canada, l’UE, l’Australie et le Brésil. Par conséquent, si nous voulons commercialiser de tels dispositifs médicaux électriques, il est important de mettre en œuvre ces normes, en respectant les exigences décrites, afin de pouvoir les commercialiser avec succès.
Ainsi, tout équipement médical électrique doit fonctionner conformément à la norme EN IEC 60601-1 pour respecter les normes de sécurité requises. EN 60101-1 détermine les exigences générales, les tests de sécurité de base et les performances des dispositifs électromédicaux.
C’est également la première partie d’un groupe de normes couvrant les performances essentielles, la compatibilité électromagnétique et la sécurité des équipements et systèmes médicaux. À son tour, la norme collatérale EN 60601-1-2, sur la sécurité de base et les performances essentielles des équipements et systèmes médicaux en présence de perturbations électromagnétiques émises par ces équipements et systèmes, est cruciale.
C’est cette norme qui traite des problèmes potentiels pour les fabricants de dispositifs électromédicaux en raison de la compatibilité électromagnétique des équipements et systèmes électromédicaux.
Une certification clé dans l’industrie
Se conformer aux normes et réglementations de qualité et de conception nécessite beaucoup de travail et fait la différence pour le succès des dispositifs médicaux. C’est pourquoi il est important d’avoir le meilleur équipement hospitalier. Un secteur dans lequel, chez Tedisel Medical, nous avons plus de 25 ans d’expérience dans la fabrication d’équipements hospitaliers pour les zones d’hospitalisation, les zones critiques et les blocs opératoires.
Notre projection internationale se distingue par la variété et l’adaptabilité de nos produits, notamment pour la fabrication de têtes de lit, de suspensions pour les unités de soins intensifs, de colonnes, de panneaux et de logiciels pour les salles d’opération.
En les utilisant dans les établissements de santé, nous parvenons également à faciliter les audits pour obtenir les principales certifications de santé.
En bref, chez Tedisel, nous attachons également une grande importance à suivre les bonnes pratiques et à nous tenir au courant de chacune des normes et certifications spécifiques du secteur de la santé afin d’offrir le meilleur produit à nos clients.









